
Az öregedést meghatározó tényezők: II. Telomerek kopása
Az öregedés egyik meghatározó tényezője a telomerek fokozatos rövidülése, amely a sejtek osztódásával párhuzamosan zajlik, és jelentős hatással van a szövetek regenerációs képességére. A telomerek kopása idővel a sejtek működésének leállásához és az öregedéssel összefüggő betegségek kialakulásához vezethet.
Az alábbi cikkben részletesen bemutatjuk a telomer rövidülés mögötti biológiai folyamatokat, valamint azokat a lehetőségeket, amelyekkel lassítható ez a folyamat.
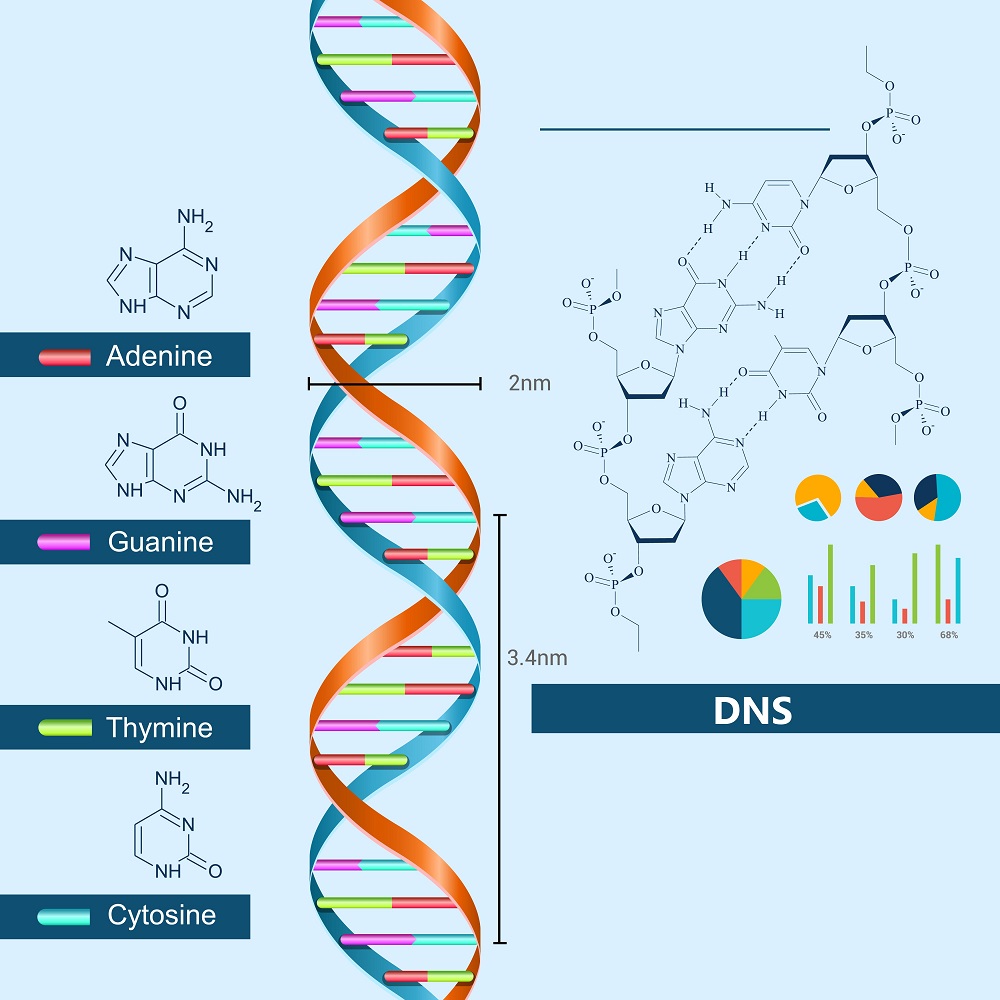
Testünk szinte minden sejtjének sejtmagjában megtalálható a DNS, vagyis a dezoxiribonukleinsav, amely az öröklött genetikai információ hordozója, és 23 pár kromoszómából áll. A kromoszómák végén található egy speciális szakasz, a telomer. A telomerek nem kódolnak fehérjéket vagy más funkcionális molekulákat, hanem védelmi szerepet töltenek be: megóvják a DNS-t a károsodástól és a sejtosztódás során bekövetkező veszteségektől.
Minden egyes sejtosztódás alkalmával, amikor a DNS megkettőződik, a telomerek fokozatosan rövidülnek. A sejtek csak meghatározott számú osztódásra képesek, mivel a telomerek fokozatos rövidülése végül eléri egy a kritikus pontot, amikor a sejtek elveszítik osztódási képességüket, és működésük leáll. Ezt a sejtosztódási korlátot Leonard Hayflick fedezte fel, és azóta Hayflick-határként ismert.
A telomerek kimerülése megmagyarázza, hogy a sejtek miért rendelkeznek véges osztódási potenciállal, és ennek következményeként miért csökken a szövetek regenerációs képessége az életkor előrehaladtával. Hayflick kísérletei kimutatták, hogy egy átlagos emberi sejt körülbelül 52 alkalommal képes osztódni, mielőtt elérné ezt a természetes határt.
Telomeráz:
Léteznek bizonyos sejtek, amelyek mentesek a telomerek rövidülésének problémájától, köszönhetően egy különleges enzimnek, a telomeráznak, amely képes újra meghosszabbítani a telomereket. Ez az enzim lényegében „halhatatlanságot” biztosít a sejtek számára. Felmerül a kérdés: ha a tudósok képesek lennének ezt az enzimet minden sejtbe bejuttatni, vajon megállíthatnánk az öregedést? A válasz azonban – ahogy a tudományban gyakran tapasztaljuk – ennél jóval összetettebb, hiszen a természet nem véletlenül döntött úgy, hogy nem lát el minden sejtet telomeráz termelő képességgel.
Sejtjeink DNS-ét folyamatosan érik külső és belső hatások, amelyek veszélyeztetik annak stabilitását. Ennek eredményeként a testünkben másodpercenként számtalan DNS-mutáció és változás következik be. Bár a sejtek rendkívül fejlett javítómechanizmusokkal rendelkeznek, amelyek a legtöbb hibát képesek korrigálni, nem mindegyiket sikerül kijavítani.
És itt rejlik a kihívás: ha ezek a javítatlan genetikai hibákat hordozó sejtek telomerázhoz jutnának, korlátlanul osztódhatnának. Az eredmény? Egyre több mutálódott, működésképtelen sejt felhalmozódása – amit jól ismerünk rák néven. A telomeráz tehát egy kétélű fegyver: míg képes lehet meghosszabbítani az életet, egyúttal fokozhatja a rosszindulatú sejtek terjedésének kockázatát is.
A telomerázt termelő sejtek közé tartoznak például az őssejtek és a csontvelősejtek, amelyek a szervezet stratégiailag védett területein találhatók. Ezek a sejtek kiemelt fontosságúak, hiszen nélkülözhetetlenek a szövetek regenerációjához és az egészség fenntartásához. Éppen ezért a természet számos védelmi mechanizmust épített ki annak érdekében, hogy minimalizálja a DNS-t érő káros hatásokat.
Az ilyen sejtek különleges tulajdonságokkal és hatékony védelmi rendszerekkel rendelkeznek, amelyek jóval eredményesebbek a legtöbb más sejt védelmi mechanizmusánál. Ennek köszönhetően a degeneráció, vagyis a kóros sejtműködés és a mutációk kialakulásának esélye jelentősen csökken.
A telomeráz jelenléte ezekben a sejtekben elengedhetetlen az egészséges szövetek folyamatos megújulásához, ugyanakkor szigorúan szabályozott környezetben működik. Ez a szabályozás biztosítja, hogy a sejtek ne osztódjanak kontrollálatlanul, ezzel minimalizálva a mutációk és a rákos elváltozások kialakulásának kockázatát.
Noha a telomeráz ígéretes lehetőségeket rejt az öregedési folyamatok lassításában, a tudomány számára továbbra is kulcsfontosságú, hogy megtalálja az egyensúlyt az élettartam növelése és a rák kialakulásának megelőzése között.
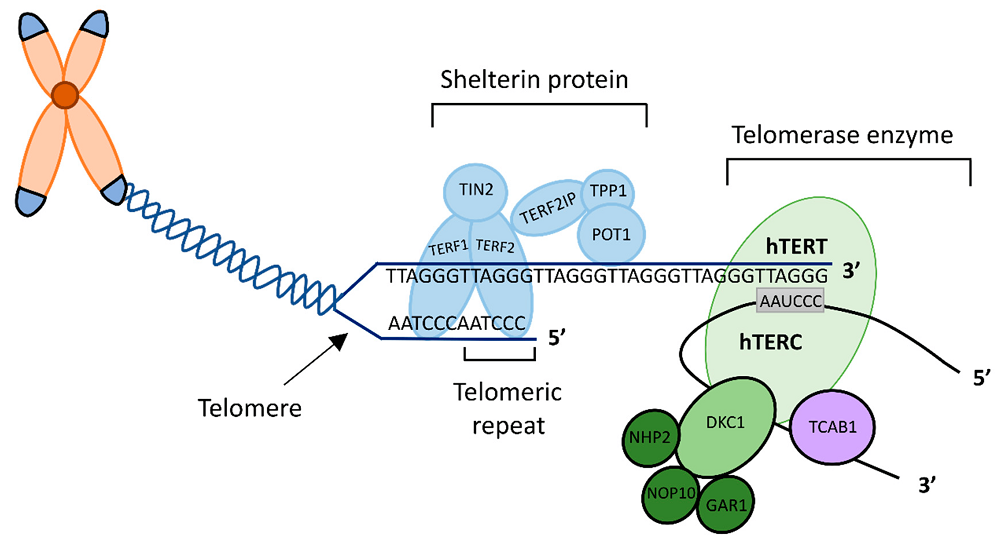 Shelterin
Shelterin
Ahogyan sok más esetben, a természet ebben is gondoskodik a szervezet védelméről: az emberek és számos más élőlény rendelkezik egy különleges mechanizmussal, amely a telomerek épségét óvja. Ezt a védelmi rendszert a shelterin nevű fehérjekomplex látja el és a telomerekhez kötődve megóvja azokat a sejt saját javítómechanizmusaitól. Ez a „védőpajzs” kulcsszerepet játszik a kromoszómák épségének megőrzésében és a sejtek korai degenerációjának megelőzésében – feltéve, hogy megfelelően működik.
Bár a shelterin hatékony védelmet biztosít, a telomerek mégsem védettek teljes mértékben a DNS-károsodással szemben, különösen a genetikai instabilitás miatt bekövetkező hatásokkal szemben. Mivel a shelterin elrejti a telomereket a sejtek javítómechanizmusai elől, az itt keletkező sérülések nem kerülnek kijavításra. Ez elsőre aggasztónak tűnhet, hiszen a felhalmozódó károsodások idővel komoly problémákhoz vezethetnek, például szeneszcenciához – egy olyan köztes állapothoz, amelyben a sejtek már nem képesek osztódni, de még nem pusztulnak el –, vagy akár programozott sejthalálhoz (apoptózishoz).
Szerencsére a telomerek területén bekövetkező DNS-károsodások általában kevésbé súlyosak, mivel ezek a régiók nem kódolnak fehérjéket, tehát nem tartalmaznak közvetlenül az életfolyamatokhoz szükséges genetikai információt. Ez azt jelenti, hogy a telomerek sérülése kevésbé befolyásolja a szervezet működését, mint a kromoszómák egyéb, génkódoló szakaszaiban bekövetkező mutációk.
A rövid telomerek kockázata
A szövetek regenerációs képességének csökkenése komoly egészségügyi kihívásokat jelent, és kutatások igazolták, hogy a rövid telomerek jelentősen növelik a korai halálozás kockázatát. Ez rávilágít arra, hogy a telomerek hossza nem csupán az öregedési folyamat természetes velejárója, hanem alapvető szerepet játszik az egészség és a hosszú élettartam megőrzésében.
Ezek az eredmények kiemelik annak fontosságát, hogy a telomeráz enzim és a shelterin fehérjekomplex megfelelő működése elengedhetetlen a sejtek és szövetek egészségének fenntartásában, valamint az öregedéssel összefüggő betegségek megelőzésében.
 Mit tehetünk addig?
Mit tehetünk addig?
Amíg a tudomány a telomerhosszabbító terápiák lehetőségeit kutatja, érdemes megvizsgálni azokat a módszereket, amelyek bizonyítottan hatékonyak az emberek esetében.
A magnézium-anyagcsere alapvető szerepet tölt be a telomerek egészségének megőrzésében. Ez az esszenciális ásványi anyag számos létfontosságú biológiai folyamatban részt vesz és elengedhetetlenek a telomerek stabilitásához és működéséhez. Egyes tanulmányok arra mutattattak rá, hogy az alacsony magnéziumszint – különösen, ha magas homocisztein-szinttel párosul – a telomerek fokozott rövidülését eredményezi.
Ha alaposabban megvizsgáljuk a telomerek és a másodlagos növényi anyagok közötti kapcsolatot, hamar eljutunk a sirtuinekhez. Ezeket a fehérjéket gyakran az „hosszú élet génjeiként” emlegetik. A sirtuinek aktiválása többféle módon lehetséges. Az egyik legismertebb természetes serkentőjük az időszakos böjt, amely bizonyítottan jelentősen növeli ezeknek a fehérjéknek a szintjét. Emellett bizonyos másodlagos növényi vegyületek, például a rezveratrol, szintén hatékonyan fokozzák a sirtuinek működését.
A magas sirtuin szint számos előnyt kínál: hozzájárul a DNS védelméhez, segít megőrizni a telomerek stabilitását, és jelentős hatást gyakorol az epigenetikai folyamatokra, vagyis a gének működésének szabályozására.
Ezek az összefüggések rámutatnak arra, hogy az életmódbeli tényezők, például a megfelelő étrend és a böjt, fontos szerepet játszhatnak a sejtek öregedésének lassításában és a hosszabb, egészségesebb élet elősegítésében.
Források
https://www.mdpi.com/1422-0067/23/2/626
https://pubmed.ncbi.nlm.nih.gov/26785477/
https://pubmed.ncbi.nlm.nih.gov/15574496/
https://pubmed.ncbi.nlm.nih.gov/36599349/
https://pubmed.ncbi.nlm.nih.gov/29210129/











