
NAD+ és CD38: két kulcsmolekula az öregedés ellen
Az öregedés egyik legérdekesebb és legintenzívebben kutatott területe a sejtek szintjén zajló energia- és anyagcsere-folyamatok, melyek középpontjában egy kulcsfontosságú molekula, a NAD+ (nikotinamid-adenin-dinukleotid) áll. A NAD+ szintje az életkor előrehaladtával drámaian csökken, ami számos öregedéssel kapcsolatos probléma forrása, beleértve a mitokondriális funkciók romlását, a DNS-javító mechanizmusok gyengülését és a sejtek energiaellátásának zavarából eredő fáradtságot.
Az utóbbi években nagy hangsúlyt kaptak az olyan NAD+ előanyagok, mint például az NMN (nikotinamid-mononukleotid) és az NR (nikotinamid-ribozid), amelyek kiegészítése hatásosan növelik a NAD+ szintet a sejtekben, hozzájárulva az öregedési folyamatok lassításához.
Azonban egy másik, ígéretes megközelítés is létezik a NAD+ szint fenntartására, amely nem a pótlásra, hanem a NAD+ szint megőrzésére fókuszál a CD38 blokkolásán keresztül. A CD38 egy olyan enzim, amely lebontja a NAD+-t, így gátlása megakadályozhatja a NAD+ jelentős veszteségét.
Mi az a CD38?
A CD38 (Cluster of Differentiation 38) enzim egy glikoprotein, amely többek között a T- és B-sejtek felszínén található. A CD38 működése során NAD+ molekulákat használ fel, miközben ADP-ribózt állít elő, ami létfontosságú a sejtek közötti kommunikációban. Azonban az életkor előrehaladtával jelentkező krónikus, alacsony szintű gyulladás (inflammaging) jelentősen fokozza a CD38 aktivitását, és ennek az enzimnek a működésében az egyik legaggasztóbb tényező, hogy rendkívül nagy mennyiségű NAD+-t fogyaszt. Pontosabban, 100 NAD+ molekulára van szüksége ahhoz, hogy egyetlen molekula ADP-ribózt állítson elő.
A kutatások kimutatták, hogy a CD38 szintjének emelkedése szoros kapcsolatban áll az öregedő sejtek által kibocsátott szeneszcens sejt-szekréciós fenotípusokkal (Senescence-Associated Secretory Phenotype, SASP). Ezek a sejtek magas gyulladáskeltő molekulákat bocsátanak ki, ami jelentősen hozzájárul a szövetek öregedéséhez és az öregedéssel kapcsolatos betegségek kialakulásához.
Mi az a NAD+?
A NAD+ (nikotinamid-adenin-dinukleotid) egy olyan koenzim, amely minden élő sejtben jelen van, és alapvető szerepet játszik a sejtek energiaellátásában és anyagcseréjében. Ez a koenzim kulcsfontosságú az elektronok szállításában, amelyek a sejtlégzés során mozognak: a NAD+ elektronokat vesz fel, majd NADH formában leadja azokat, hogy újra felvegye. Ez az elektrontranszfer létfontosságú az ATP, a sejtek fő energiamolekulájának termeléséhez. Az ATP biztosítja az energiát minden sejt számára, és a mitokondriumokban keletkezik.
A NAD+ szintjének fenntartása kritikus, mivel nemcsak az ATP-termelésben játszik központi szerepet, hanem számos egyéb létfontosságú funkcióban is. Ilyen például a DNS-javítás, a sejtek metabolizmusának szabályozása, valamint a sirtuinok aktiválása. A sirtuinok olyan fehérjék, amelyek számos öregedéshez kapcsolódó folyamatot szabályoznak, beleértve a sejtvédelmet és a gyulladásgátlást. Ezen funkciók mind kulcsszerepet játszanak az öregedés késleltetésében és a sejtek hosszú távú egészségének megőrzésében.
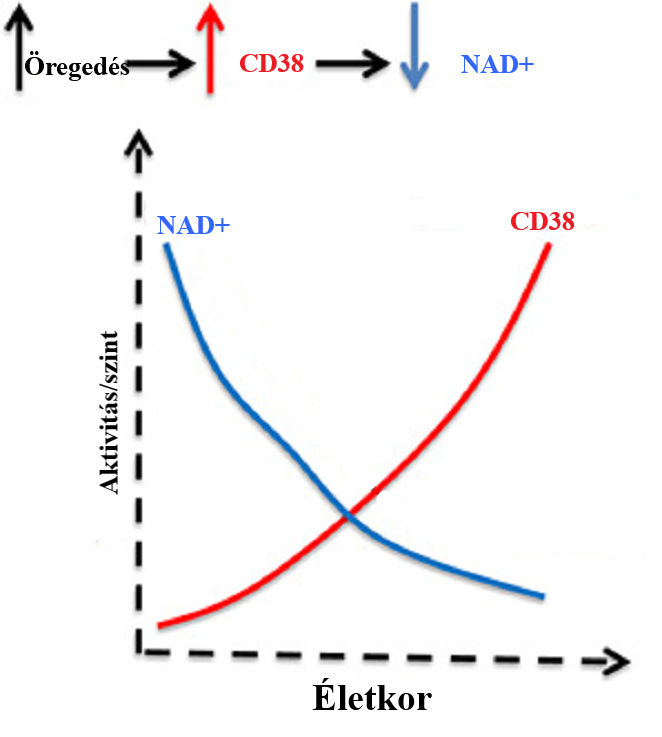
CD38 és NAD+
Ahogy öregszünk az öregedő sejtjeink fokozatosan felhalmozódnak, és egyre több gyulladásos választ váltanak ki. A gyulladás normális esetben a szervezet védekező reakciója a kórokozók elleni küzdelemben, valamint a szövetek javításában és fenntartásában játszik szerepet. Ha rövid ideig tart, hasznos lehet, azonban ha folyamatosan fennáll, krónikussá válik, és káros hatással van a szervezetünkre. Az emberek többségénél az öregedés együtt jár egy alacsony szintű, krónikus gyulladással, amely annyira általános tünete az öregedésnek, hogy gyakran "gyulladásos öregedésnek" (inflammaging) is nevezik.
Normális körülmények között a gyulladás és a CD38 aktivációja átmeneti, de ahogy az öregedő sejtek száma növekszik, ezek a sejtek fokozott gyulladást váltanak ki, ami a CD38 enzim tartós és túlzott aktivációjához vezet. Ez a folyamat hozzájárul a NAD+ szint életkorral összefüggő csökkenéséhez. Itt egy ördögi kör alakul ki: ahogy a NAD+ szint csökken, még több öregedő sejt jelenik meg, amelyek tovább aktiválják a CD38-at, ami még több NAD+-t merít ki. Beavatkozás nélkül ez a ciklus fokozatosan gyorsítja az öregedési folyamatot, és súlyosbítja annak hatásait.
 A CD38 aktivitása csökkenthető?
A CD38 aktivitása csökkenthető?
Állatkísérletek során bebizonyosodott, hogy amikor a CD38 termelését részben gátolták, az alanyok meg tudták őrizni NAD+ szintjüket, ami egyben bizonyítja is, hogy a CD38 kulcsszerepet játszik a NAD+ szint csökkenésében.
Ezek a felfedezések rendkívül biztatóak, mert azt mutatják, hogy a CD38 aktivitásának gátlásával lehetséges az öregedési folyamatok lassítása. Bár a CD38 teljes blokkolása káros lehet, mivel bizonyos sejtfunkciókat megzavarhat, a részleges gátlása hatékony és ígéretes megközelítés.
Két természetes vegyületről, az apigeninről és a kvercetinről kimutatták, hogy képesek mérsékelni a CD38 túlzott aktivitását. Egérkísérletekben például az apigenin 75%-kal növelte a NAD+ szintet, míg a kvercetin 30%-os növekedést eredményezett, ami további bizonyítékot szolgáltat ezen vegyületek hatékonyságára.
- Az apigenin egy polifenol, amely számos növényben megtalálható, például a petrezselyemben, kamillában, vörösborban, sörben, zellerben és oregánóban. A legnagyobb koncentrációban a szárított petrezselyem tartalmazza. A hőkezelés azonban jelentősen csökkenti az Apigenin mennyiségét, így alternatív megoldásként étrend-kiegészítő formában is szedhető, ami kényelmesebb lehet a megfelelő mennyiség eléréséhez.
- A kvercetin szintén egy polifenol, amely olyan élelmiszerekben található meg, mint az alma, méz, málna, vöröshagyma, szőlő, citrusfélék és levélzöldségek. A kutatások azt mutatják, hogy napi 500 mg és 1 gramm közötti kvercetin bevitel jelentősen gátolhatja a CD38 enzimet, és ezáltal növelheti a NAD+ szintet-
Ezek az eredmények arra utalnak, hogy ezeknek a polifenoloknak a rendszeres fogyasztása, akár étrend-kiegészítők, akár táplálékforrások révén, potenciálisan késleltethetik az öregedést, javítva a sejtek energia- és anyagcsere-folyamatait.
Forrás:
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3609577/










